

更新时间 2024-05-07 10:50:26
北京大学第一医院张宁、北京大学肿瘤医院吴健民及郑州大学附属肿瘤医院/河南省肿瘤医院张建功等人使用肝癌患者组织样本构建了肝癌类器官生物库,以适用于药物敏感性筛选,并对肝癌异质性进行剖析。此外,他们揭示了仑伐替尼的耐药机制,并依此开发新的化合物弥补其不足之处,为肝癌精准治疗提供了重要线索。
首先,研究团队通过从144名肝癌患者的手术样本中采集多区域组织,建立了一个包含399个肿瘤类器官的肝癌类器官生物库。这些类器官在基因组和转录组水平上与原肿瘤组织高度一致,为深入研究肝癌的异质性和开发针对性治疗提供了重要工具。
基于肝癌类器官生物库,研究团队鉴定出大量基因组异质性,为患者构建肿瘤细胞进化树。此外,通过使用药物处理患者的类器官培养物,发现索拉非尼、仑伐替尼的治疗靶点在瘤内多区域差异表达,且表达较低的区域表现出较高的耐药性,表明基因表达水平的不一致可能是导致治疗效果差异的一个因素。
接下来,研究团队在来自肝癌患者的类器官模型上进行了药物筛选,包括原发性肝癌的一线药物索拉非尼、仑伐替尼,二线药物瑞戈非尼、阿帕替尼,抗VEGFR抗体贝伐珠单抗,以及肝胆癌靶向药佩米替尼。
类器官模型的药物敏感性测试结果与患者的临床反应比较,显示了高度的一致性,支持此次构建的类器官模型在预测患者对特定药物治疗反应方面的潜在价值,甚至有可能指导个性化医疗和治疗决策。举例来看,某位患者对索拉非尼和经导管动脉化疗栓塞治疗无反应,但随后接受仑伐替尼治疗后达到完全缓解,持续5个月;与临床反应一致,这位患者的所有三种类器官均被发现对索拉非尼具有耐药性,但对仑伐替尼敏感。
类器官模型得出的药物敏感性测试结果也在异种移植瘤小鼠实验中得到验证。
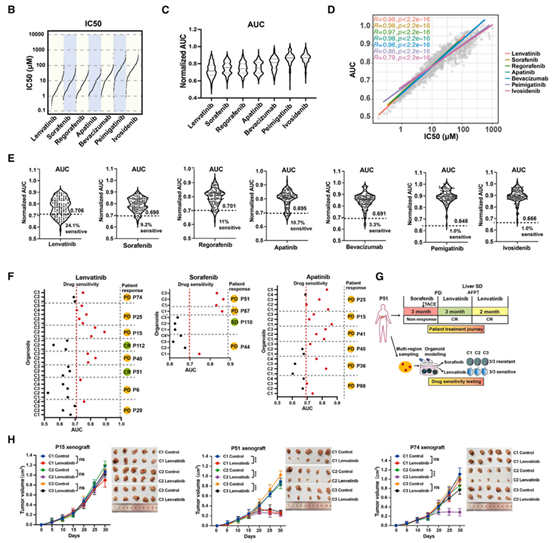
可预测患者反应并揭示肿瘤内药物敏感性的异质性
使用基于机器学习的方法,研究团队成功识别了13个关键基因作为预测仑伐替尼治疗反应的生物标志物,展现出良好的效能(训练集和验证集的AUROC值为0.86和0.81)。同样的方法也被应用于索拉非尼、瑞戈非尼、阿帕替尼,每种药物的预测效能均表现出较高的AUROC值。
最后,研究团队重点探讨了仑伐替尼的肝癌耐药机制以及应对策略。他们发现,高水平的c-Jun蛋白通过影响Wnt/β-catenin和JNK信号通路,与仑伐替尼耐药有关,c-Jun抑制剂与仑伐替尼联合使用时具有协同效应。
于是,研究团队参考c-Jun抑制剂与仑伐替尼的协同效应,开发了新的化合物PKUF-01,旨在靶向c-Jun和FGFRs。在患者来源的类器官中验证效果,显示PKUF-01能有效克服仑伐替尼的耐药性;异种移植瘤小鼠实验结果显示,PKUF-01单独治疗(每日1次,每次10 mg/kg)比仑伐替尼单独治疗更有效地抑制肿瘤生长。
此外,研究还利用机器学习方法开发一组多基因签名,用以预测对PKUF-01的治疗反应训练集和验证集的AUROC值为0.836和0.731,显示出良好的预测性能。通过分析肝癌类器官生物库,研究团队表明,PKUF-01在治疗原发性肝癌方面的疗效显著优于单独使用仑伐替尼(54.0% vs 42.6%),并能使更多肝癌患者受益(34.5% vs 24.1%);当PKUF-1与上述七种已获批药物联合使用时,48.3%的患者可从中受益。
本研究探讨了原发性肝癌中仑伐替尼的耐药性机制,并开发了新化合物PKUF-01以克服此耐药性。通过靶向c-Jun蛋白和相关信号通路,PKUF-01治疗肝癌极具潜力。这些成果为肝癌的个性化治疗提供了新策略,加速肝癌的精准医疗。
关于好安森糖尿病治疗仪

好安森糖尿病治疗仪系出“人民健康家庭系统工程”,属于“四大系统工程”之一的“有序生命信息场工程”。好安森糖尿病治疗仪运用“钱学森系统学原理”,由好安森首席科学家何月蓉院士团队领衔科研攻关,倾尽心血打造,是“中医现代化”成果产品之一。
参考文献:
[1]https://www.cell.com/cancer-cell/fulltext/S1535-6108(24)00089-8