

更新时间 2024-03-26 16:23:24
先前的研究表明,二甲双胍的减肥功效要归因于其抑制食欲的特性,比如:诱导肝细胞表达并分泌“厌食激素”生长与分化因子15(GDF15),进而调节大脑特定区域来抑制对高脂饮食的欲望。但这并非唯一或者最主要的途径,而背后的其他机制仍不明确。
这个问题终于有答案了。Nature Metabolism上接连刊登两篇论文给出了解答:N-乳酰苯丙氨酸(Lac-Phe)是二甲双胍“减肥”作用中的关键一环。具体来说,二甲双胍通过抑制复合物I、增加糖酵解通量和细胞内乳酸质量作用来促进Lac-Phe的生物合成;而代谢物Lac-Phe具有抑制食欲的作用,从而实现体重的减轻。
这两项研究分别从机制探究和人群试验入手,全方位地解读了“二甲双胍是如何发挥减肥作用”的。而早在2022年就有研究发现,剧烈运动抑制食欲的“始作俑者”也是Lac-Phe;换言之,二甲双胍和剧烈运动的减肥机制可谓是“异曲同工之妙”。

https://doi.org/10.1038/s42255-024-01018-7

https://doi.org/10.1038/s42255-024-00999-9
Lac-Phe是肌肽酶2(CNDP2)产生的一种代谢物,能催化乳酸和苯丙氨酸的融合作用。之前的动物实验显示,给肥胖小鼠注射Lac-Phe能够有效地抑制食欲;而类似的情况也出现在人类试验中,经常运动所致的体重减轻也与Lac-Phe有关。
于是,Lac-Phe引起了研究者的关注。该化合物是否为二甲双胍抑制食欲过程中的重中之重呢?
在第一篇基于人群试验的论文中,研究者整理了7项观察性和干预性研究后发现,服用二甲双胍的受试者血液中Lac-Phe水平显著升高,从而抑制食欲的产生。
举例来说,研究者从哈佛大学附属医院布列根和妇女医院中收集到33名志愿者的血清样本,并使用高效液相色谱-串联质谱(UPLC-MS/MS)量化了1168个血清代谢物。数据显示,与肥胖的非2型糖尿病(T2D)志愿者相比,肥胖的T2D患者体内所有测得的N-乳酰基氨基酸均明显增加;即这种增加与BMI无关,而与T2D状态有关。
鉴于Lac-Phe的食欲抑制特性,研究者专注于这种特殊的N-乳酰基氨基酸。很有意思的是,与肥胖的非T2D对照组相比,肥胖的T2D患者体内的Lac-Phe水平是前者的5.7倍。此外,肥胖T2D和糖尿病前期的个体中,Lac-Phe含量也明显增加。
那么,为什么T2D患者血液中Lac-Phe水平会明显呢?考虑到二甲双胍在T2D患者中的广泛使用性,研究者分析了二甲双胍和Lac-Phe两者之间的相关性,计算得到的斯皮尔曼(Spearman)相关系数为0.76,即两者之间存在强相关性。
与此同时,研究者发现在停止服用二甲双胍的T2D患者中,Lac-Phe水平降到最低值。这一发现再次证明,T2D患者血清中Lac-Phe水平的增加是由二甲双胍而非T2D本身引起的。
除了T2D患者队列外,研究者同样还在健康人群观察到“二甲双胍能够增加Lac-Phe水平”。
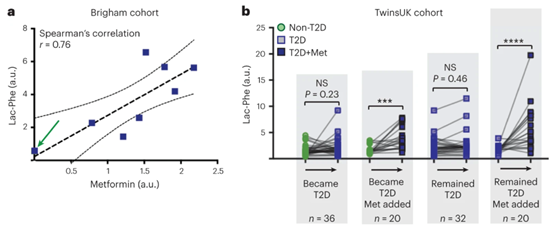
二甲双胍治疗增加Lac-Phe水平
综上,这项研究总结了TwinsUK队列、丹麦二甲双胍干预研究队列等等7个人群研究,发现:二甲双胍能够增加血清中Lac-Phe水平,从而发挥抑制食欲的作用;而Lac-Phe的升高是二甲双胍治疗特异性的,与T2D状态无关。
如果说人群试验只停留在“表面”,第二篇研究则从细胞、小鼠实验和独立人类队列多角度切入,进一步揭秘了二甲双胍的具体作用链路。
事实上,肠上皮CNDP2+细胞是Lac-Phe的主要生产源。于是,斯坦福大学医学院的研究团队开展了小鼠实验,他们敲除了小鼠的CNDP2基因后发现,即使这些小鼠服用了二甲双胍,依然会持续摄入食物且体重未发生改变。
此外,研究者还在小鼠实验中观察到了整个链路:二甲双胍能通过抑制复合物I、增加糖酵解通量和细胞内乳酸质量作用来促进Lac-Phe的生物合成,从而发挥抑制食欲的作用。但目前Lac-Phe下游信号通路还未被完全破解,亟需更多研究的开展。
不过,该研究的领头人Jonathan Long教授对此持乐观态度。他表示,通过优化口服药物二甲双胍,或能成功地控制体重、胆固醇和血压;而上述发现也为更安全、更有效的新型减肥药物的开发铺路。
关于好安森糖尿病治疗仪

好安森糖尿病治疗仪系出“人民健康家庭系统工程”,属于“四大系统工程”之一的“有序生命信息场工程”。好安森糖尿病治疗仪运用“钱学森系统学原理”,由好安森首席科学家何月蓉院士团队领衔科研攻关,倾尽心血打造,是“中医现代化”成果产品之一。
参考资料:
[1]Xiao, S., Li, V.L., Lyu, X. et al. Lac-Phe mediates the effects of metformin on food intake and body weight. Nat Metab (2024). https://doi.org/10.1038/s42255-024-00999-9
[2]Scott, B., Day, E.A., O’Brien, K.L. et al. Metformin and feeding increase levels of the appetite-suppressing metabolite Lac-Phe in humans. Nat Metab (2024). https://doi.org/10.1038/s42255-024-01018-7