

更新时间 2023-11-07 16:40:48
糖尿病是诱发胰腺癌的危险因素之一,胰腺癌可伴发糖尿病。糖尿病人应将血糖控制在正常范围内,以降低胰腺癌的发病率,胰腺癌患者需要定期监测血糖,以辅助治疗。国外一项研究结果表明,糖尿病人的胰腺癌发病率较正常人要高出1.5到7倍。但是,糖尿病如何诱导胰腺癌的发生,机制并不清楚。
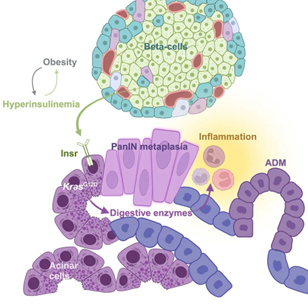
近日,一项研究成果揭示了胰岛素水平升高诱发胰腺癌的关键机制:胰岛素水平升高可直接诱导胰腺内,一部分表达胰岛素受体、且存在KRAS突变的腺泡细胞转化为胰腺上皮内瘤变(PanIN),即胰腺癌的关键癌前病变。该研究由加拿大麦吉尔大学和不列颠哥伦比亚大学的研究者们证实,发布在Cell Metabolism期刊上。
这部分腺泡细胞对人体的血糖调节无足轻重,但在胰岛素作用下,它们会通过诱导局部炎症、增加胰腺消化酶蛋白的翻译等机制,促进PanIN及腺泡到导管化生(ADM)的发生,因此由胰岛素/胰岛素受体调控的这种促癌作用不容小视。
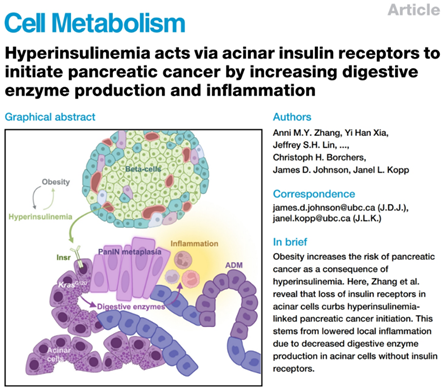
论文核心内容总结
为了验证胰岛素/胰岛素受体通路在胰腺癌发生发展中的作用,研究者们首先用高脂饮食(HFD)喂养+他莫昔芬处理(诱导KRASG12D突变)构建了小鼠模型,并证实敲除胰腺腺泡细胞的胰岛素受体表达,并不会扰乱血糖稳态。而由KRASG12D突变导致的胰腺实质丢失,也可在敲除胰岛素受体后被部分逆转。
进一步分析显示,敲低或敲除胰岛素受体,确实可以减少PanIN及后续癌变,即胰腺导管腺癌(PDAC)的数量,且这种抑制作用主要体现在PanIN发生发展的早期(小鼠12周龄),即早早把胰腺癌扼杀在萌芽阶段,可能被胰岛素受体激活的促癌下游信号通路PI3K/AKT/mTOR、MAPK/ERK活性也相应下降。
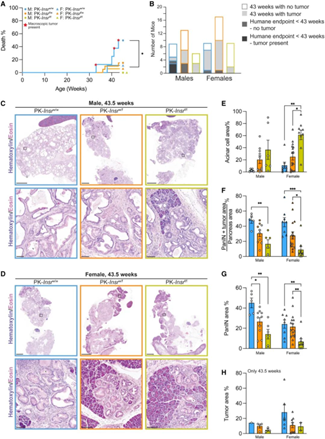
敲除腺泡细胞的胰岛素受体,可减少PanIN的形成
但研究者们认为,胰岛素受体的作用还不限于激活已知的上述信号通路,因此又展开了蛋白组学和磷酸化组学层面的分析,发现在敲除胰岛素受体后,腺泡细胞内与PanIN形成相关的多种蛋白显著富集,这与此前的实验结果一致。
但组学分析的后半部分结论,就出乎研究者们的预料了:敲除胰岛素受体后,腺泡细胞内常规被封装到酶原颗粒中,再外排的多种消化酶蛋白水平都出现了显著下调,且这种调节是对消化酶合成的转录后调节。
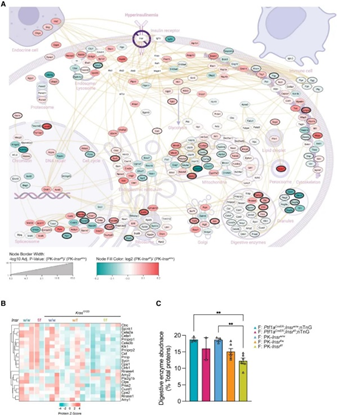
敲除胰岛素受体后,腺泡细胞内消化酶显著减少
而胰岛素水平升高、胰岛素受体存在时,增多的消化酶们显然就与PanIN形成和炎症等促癌机制有关了:胰岛素水平升高时,胰蛋白酶原的自我催化会促进消化酶分泌,在胰腺内带起更广泛的促癌炎症和PanIN形成;磷酸化组学分析还显示,胰岛素水平升高可能通过调控特定转录因子、RNA剪接等机制促癌。
那么抑制胰岛素/胰岛素受体通路,能在多大程度上减少癌变风险呢?染色实验显示在敲除胰岛素受体、仅存留KRASG12D突变的情况下,KRAS突变诱导的胰腺纤维化和炎症水平会明显减弱,PanIN和ADM也相应少了。
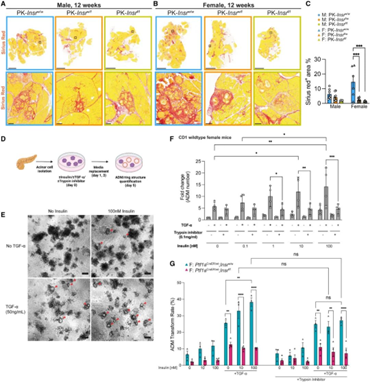
抑制胰岛素/胰岛素受体通路,可减轻胰腺纤维化和炎症水平
总而言之,本次研究揭示了胰岛素/胰岛素受体通路在胰腺腺泡细胞癌变和胰腺癌发生早期的重要作用,而从中受益的或许不仅有胰腺癌的治疗,未来的胰腺癌早期筛查也可能发生变革,检测胰岛素水平而非血糖水平可能才是关键。
关于好安森糖尿病治疗仪

好安森糖尿病治疗仪系出“人民健康家庭系统工程”,属于“四大系统工程”之一的“有序生命信息场工程”。好安森糖尿病治疗仪运用“钱学森系统学原理”,由好安森首席科学家何月蓉院士团队领衔科研攻关,倾尽心血打造,是“中医现代化”成果产品之一。
参考文献:
[1]Zhang A M Y, Magrill J, de Winter T J J, et al. Endogenous hyperinsulinemia contributes to pancreatic cancer development[J]. Cell Metabolism, 2019, 30(3): 403-404.
[2]Zhang A M Y, Xia Y H, Lin J S H, et al. Hyperinsulinemia acts via acinar insulin receptors to initiate pancreatic cancer by increasing digestive enzyme production and inflammation[J]. Cell Metabolism, 2023.